NỘI DUNG
Thử nghiệm thủy phân tinh bột (Starch hydrolysis test) để xác định khả năng phân hủy tinh bột thành maltose thông qua hoạt động của enzyme α-amylase ngoại bào hay không.
Thử nghiệm thủy phân tinh bột
Tinh bột, nguồn carbohydrate quan trọng nhất với con người, là hỗn hợp polysacarit của hai polyme, amyloza và amylopectin.
Amylose là một polysaccharide mạch thẳng gồm vài nghìn α-D-glucose được liên kết bằng liên kết 1,4-α-glycosid. Amylopectin là một polysaccharide chuỗi nhánh gồm các đơn vị glucose được liên kết chủ yếu bằng liên kết α-1,4-glycosid. Nhưng thỉnh thoảng có liên kết α-1,6-glycosid, chịu trách nhiệm phân nhánh.
Nguyên tắc thử nghiệm thủy phân tinh bột
Các phân tử tinh bột quá lớn để đi vào tế bào vi khuẩn nên chỉ có vi khuẩn tiết ra exoenzym (α -amylase và oligo-1,6-glucosidase) mới có thể thủy phân tinh bột thành các tiểu đơn vị (dextrin, maltose hoặc glucose). Những phân tử này được vận chuyển vào tế bào vi khuẩn để sử dụng trong quá trình trao đổi chất.
Trong thử nghiệm thủy phân tinh bột, sử dụng thạch tinh bột, một môi trường dinh dưỡng khác biệt. Các sinh vật thử nghiệm được cấy vào đĩa tinh bột và ủ ở 30°C/48h cho đến khi thấy sự phát triển. Đĩa Petri sau đó được đổ đầy dung dịch iốt.
Nếu không có enzyme nghĩa là không bị thủy phân, amyloza và iốt phản ứng tạo thành màu xanh lam. Tùy thuộc vào nồng độ iốt sử dụng, iốt chuyển sang màu xanh lam, tím, đen khi có tinh bột.
Khi vi khuẩn có khả năng sinh α-amylase và oligo-1,6-glucosidase được nuôi cấy trên môi trường thạch tinh bột. Chúng sẽ tiết ra các enzym vào vùng xung quanh và thủy phân tinh bột. Vì không có amyloza nên không có sự phát triển màu sắc xung quanh khuẩn lạc..
Cần tư vấn đào tạo ISO 17025, ISO 15189 Mời gọi 0919 099 777
Nguyên vật liệu
- Heart infusion agar (HIA) với 2% tinh bột hoặc thạch Mueller Hinton (MHA) .
- Iốt
- Que cấy vô trùng hoặc vòng cấy
Kiểm soát chất lượng
Kiểm tra thạch tinh bột xem có bị đóng băng, nhiễm bẩn, nứt và mất nước trước khi bảo quản và trước khi sử dụng.
Thực hiện kiểm soát chất lượng trên từng mẻ thạch tinh bột mới trước khi sử dụng. Kiểm tra hiệu suất của thạch bằng cách sử dụng các sinh vật thử nghiệm sau .
- S.bovisATCC 33317—quầng sáng rõ ràng xung quanh khuẩn lạc khi bổ sung iốt (dương tính với tinh bột)
- Enterococcus faecalisATCC 25922—màu xanh khi bổ sung iốt (âm tính tinh bột)
Công dụng Thử nghiệm thủy phân tinh bột
- Để phân biệt các thành viên của các chi khác nhau bao gồm Bacillus, Clostridium, Corynebacteria, Fusobacteria, Enterococcus, Pseudomonas và Streptococcus. Những chi này có cả loài amylase dương tính và amylase âm tính.
- Để tách Streptococcus bovis(dương tính) khỏi các streptococci nhóm viridans khác có mật-esculin dương tính. NaCl âm tính 6,5% và pyrrolidonyl-β-naphthylamide (PYR) âm tính.
Quy trình kiểm tra
- Chọn một vài khuẩn lạc thử nghiệm bằng cách sử dụng tăm bông hoặc que cấy vô trùng.
- Kẻ một đường trên đĩa tinh bột theo chiều rộng của đĩa. Một số chủng cấy có thể được thử nghiệm trên một đĩa thạch. Mỗi đĩa được biểu thị bằng một đường hoặc đĩa có thể được chia thành bốn góc phần tư.
- Ủ đĩa ở 37°C trong 48 giờ.
- Thêm 2-3 giọt dung dịch iốt 10% trực tiếp lên rìa khuẩn lạc. Đợi 10-15 phút và ghi lại kết quả. Đọc các đĩa ngay sau khi thêm iốt, vì màu xanh nhạt dần.
Đọc kết quả
- Thử nghiệm dương tính (“+”): Màu tím đen đặc trưng sẽ xuất hiện trong môi trường. Tuy nhiên, một quầng sáng rõ ràng sẽ xuất hiện xung quanh khuẩn lạc củacác loài dương tính với amylase. Cầu khuẩn Gram dương, Catalase âm tính, PYR âm tính, có mật esculin dương tính, không phát triển trên môi trường muối 6,5% và thủy phân tinh bột là bovis.
- Xét nghiệm âm tính (“-“): Màu tím-đen đặc trưng sẽ xuất hiện trong môi trường, ngay sát rìa các khuẩn lạc phân lập của loài amylase âm tính.
Kết quả thử nghiệm thủy phân tinh bột của các sinh vật chọn lọc
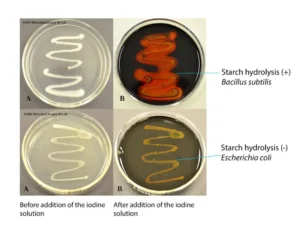
| Thủy phân tinh bột (+ve) | Thủy phân tinh bột (-ve) |
| trực khuẩn subtilis | Streptococcus agalactiae |
| trực khuẩn cereus | Staphylococcus biểu bì |
| Bacillus megaterium | Escherichia coli |
Hạn chế
- Tránh sử dụng môi trường tinh bột glucose vì quá trình chuyển hóa glucose có thể ảnh hưởng.
- Một khi iốt được thêm vào, các sinh vật sẽ không thể tồn tại được.
- Màu đỏ tím là do thủy phân một phần và thử nghiệm phải được lặp lại sau khi ủ tiếp.
Nguồn
- Archana Lal, Naowarat Cheeptham. 2012. Giao thức thạch tinh bột.
- Madigan MT, Martinko JM, Stahl DA, Clark DP. 2012. Sinh học Brock của vi sinh vật, tái bản lần thứ 13. Benjamin Cummings, San Francisco, CA.




