NỘI DUNG
So sánh kết quả xét nghiệm hay đánh giá độ tương đồng theo ISO 15189 là yêu cầu bắt buộc các phòng xét nghiệm phải thực hiện. Bài viết sau sẽ giải thích các yêu cầu 7.3.7.4 So sánh kết quả xét nghiệm theo ISO 15189:2022
Yêu cầu a
Khi sử dụng các phương pháp hoặc thiết bị khác nhau, hoặc cả hai, để xét nghiệm và/hoặc xét nghiệm được thực hiện tại các địa điểm khác nhau, phải xây dựng quy trình quy định khả năng so sánh các kết quả đối với các mẫu bệnh phẩm trong suốt các khoảng thời gian có ý nghĩa lâm sàng.
CHÚ THÍCH: Việc sử dụng các mẫu bệnh phẩm khi so sánh các phương pháp xét nghiệm khác nhau có thể tránh được những khó khăn liên quan đến hạn chế về tính dễ thay đổi của vật liệu IQC. Khi mẫu bệnh nhân không có sẵn hoặc không thực tế, hãy xem tất cả các tùy chọn được mô tả cho IQC và EQA.
Giải thích
Yêu cầu này đặt ra khi PXN thực hiện cùng một loại xét nghiệm (ví dụ: đo Glucose máu) nhưng lại dùng:
- Hai hay nhiều hơn máy xét nghiệm cùng loại hoặc khác loại
- Nhiều hơn một phương pháp đo (ví dụ: phương pháp hóa học và phương pháp điện cực chọn lọc ion).
- Thực hiện tại nhiều địa điểm khác nhau (ví dụ: phòng xét nghiệm trung tâm và phòng xét nghiệm vệ tinh).
Trong những trường hợp này, PXN phải có một quy trình rõ ràng. Quy trình này mô tả cách kiểm tra xem kết quả từ các máy, phương pháp, địa điểm khác nhau có cho ra kết quả tương đương không. Việc so sánh cần được thực hiện trên các mẫu có nồng độ khác nhau. Gồm cả các giá trị bình thường và bất thường quan trọng về mặt lâm sàng.
Lưu ý: Tiêu chuẩn khuyến khích nên dùng chính mẫu của bệnh nhân để làm so sánh này. Lý do là các mẫu QC đôi khi không phản ứng hoàn toàn giống mẫu bệnh nhân trên các máy, phương pháp khác nhau.
Nếu không thể dùng mẫu bệnh nhân, cân nhắc các phương pháp thay thế đã đề cập trong phần nội và ngoại kiểm.
Cần tư vấn đào tạo ISO 15189 mời gọi 0919 099 777
Ví dụ
PXN có một máy xét nghiệm miễn dịch A và một máy dự phòng hiệu B. Cả hai máy đều chạy xét nghiệm TSH. PXN phải xây dựng quy trình so sánh kết quả TSH giữa hai máy này. Quy trình nêu rõ: Lấy 40 mẫu máu bệnh nhân có kết quả TSH trải dài từ thấp đến cao. Phân tích mỗi mẫu trên cả máy A và máy B. Sau đó dùng hồi quy Passing-Bablok hoặc biểu đồ Bland-Altman để đánh giá độ tương đồng thiết bị.
Yêu cầu b
Phòng xét nghiệm phải ghi nhận kết quả so sánh được thực hiện và khả năng chấp nhận của kết quả đó.
Giải thích
Toàn bộ quá trình và kết quả của việc so sánh phải được ghi lại thành hồ sơ. Hồ sơ này bao gồm dữ liệu thô, kết quả phân tích thống kê, các biểu đồ nếu có. Có kết luận thiết bị, phương pháp có tương đương không. Có nằm trong giới hạn chấp nhận được mà PXN đã đề ra không.
Ví dụ
Sau khi thực hiện so sánh TSH giữa máy A và máy B, PXN ghi lại vào “Biên bản so sánh tương đương TSH – Lần 1/2025”. Biên bản có bảng dữ liệu kết quả từ hai máy, biểu đồ Bland-Altman, và kết luận: “Độ lệch trung bình (bias) giữa máy B so với máy A là +5%, giới hạn đồng ý 95% là từ -8% đến +18%. Kết quả này đáp ứng tiêu chí chấp nhận (bias < 10%, giới hạn đồng ý < 20%). Kết luận: Kết quả TSH giữa máy A và B là tương đương về mặt lâm sàng.”
Yêu cầu c
Phòng xét nghiệm phải định kỳ xem xét lại khả năng so sánh của kết quả.
Giải thích
Việc kiểm tra tính tương đương không phải chỉ làm một lần rồi thôi. Máy móc, hóa chất, quy trình có thể thay đổi theo thời gian. Do đó, PXN phải thực hiện lại việc so sánh này một cách định kỳ. Tần suất 6 tháng hay 1 năm nên được xác định dựa trên độ ổn định của các hệ thống. Kết quả xem xét định kỳ cũng phải được ghi lại.
Yêu cầu d
Khi xác định được sự khác biệt, tác động của những khác biệt đó đối với khoảng chuẩn sinh học và giới hạn quyết định lâm sàng sẽ được đánh giá và hành động.
Giải thích
Nếu trong quá trình so sánh có sự khác biệt đáng kể, vượt quá giới hạn chấp nhận. Thì phải tìm hiểu nguyên nhân. Đồng thời phải đánh giá xem sự khác biệt này có ảnh hưởng đến việc sử dụng khoảng tham chiếu hay giới hạn quyết định mà bác sĩ dùng để chẩn đoán không. Dựa trên đánh giá đó, PXN phải có hành động phù hợp. Hành động có thể là:
- Cố gắng điều chỉnh (ví dụ: chuẩn lại máy, thay đổi quy trình) để giảm sự khác biệt.
- Nếu không thể giảm khác biệt, có thể phải sử dụng khoảng tham chiếu riêng cho từng máy hoặc phương pháp.
- Quyết định chỉ dùng một hệ thống cho một số loại xét nghiệm hoặc bệnh nhân nhất định.
Ví dụ
Lần so sánh định kỳ phát hiện máy B cho kết quả TSH trung bình thấp hơn máy A 15% (vượt tiêu chí <10%).
PXN đánh giá rằng sự khác biệt này có thể ảnh hưởng đến việc theo dõi bệnh nhân suy giáp đang điều trị.
PXN tiến hành kiểm tra lại cả hai máy. Sau khi hiệu chuẩn lại, sự khác biệt giảm xuống còn 5%. PXN ghi nhận hành động khắc phục và kết quả mới đạt yêu cầu.
Yêu cầu e
Phòng xét nghiệm phải thông báo cho người sử dụng về bất kỳ sự khác biệt đáng kể nào về mặt lâm sàng trong khả năng so sánh của kết quả.
Giải thích
Trong trường hợp PXN đã cố gắng hết sức mà vẫn còn tồn tại sự khác biệt đáng kể về mặt lâm sàng giữa thiết bị hoặc phương pháp. Thì phải thông báo điều này cho bác sĩ lâm sàng. Việc thông báo này giúp bác sĩ hiểu rõ hơn về kết quả xét nghiệm. Giúp họ biết rằng kết quả từ máy này có thể khác một chút so với máy kia. Và cần cân nhắc điều đó khi diễn giải.
Ví dụ
Giả sử sau khi khắc phục ở ví dụ trước, sự khác biệt TSH vẫn còn khoảng 7%. PXN nhận thấy điều này không lớn nhưng vẫn muốn thông báo cho bác sĩ.
Kết quả TSH thực hiện trên hệ thống dự phòng (Máy B) có thể thấp hơn khoảng 5-7% so với hệ thống chính (Máy A).
Đề nghị bác sĩ lưu ý thông tin này khi theo dõi bệnh.
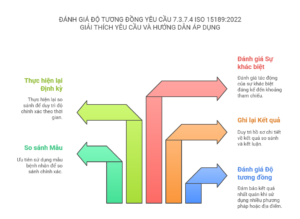
Tóm tắt yêu cầu đánh giá độ tương đồng thiết bị, yêu cầu 7.3.7.4 ISO 15189:2022
- Khi dùng nhiều hơn máy hoặc phương pháp hoặc địa điểm cho cùng xét nghiệm thì nên đánh giá độ tương đồng.
- Có quy trình rõ ràng để thực hiện việc so sánh này (cách làm, tiêu chí chấp nhận).
- Ưu tiên dùng mẫu bệnh nhân để so sánh.
- Ghi lại kết quả so sánh và kết luận có chấp nhận được không.
- Thực hiện lại việc so sánh định kỳ.
- Nếu có khác biệt lớn, phải đánh giá ảnh hưởng đến khoảng tham chiếu/ngưỡng quyết định và có hành động khắc phục.
- Thông báo cho bác sĩ nếu còn tồn tại sự khác biệt đáng kể về mặt lâm sàng.
Hồ sơ chứng minh đã tuân thủ yêu cầu so sánh tương đồng thiết bị, phương pháp
- Quy trình đánh giá độ tương đồng
- Hồ sơ đánh giá độ tương đồng(bao gồm dữ liệu thô, kết quả phân tích thống kê, biểu đồ, kết luận chấp nhận).
- Hồ sơ về việc điều tra nguyên nhân và hành động khắc phục khi phát hiện sự khác biệt không chấp nhận được.
- Hồ sơ đánh giá tác động của sự khác biệt lên khoảng tham chiếu/giới hạn quyết định lâm sàng.
- Bằng chứng về việc đã thông báo cho người sử dụng về các khác biệt có ý nghĩa lâm sàng (nếu có).
Trí Phúc
Cần tư vấn đào tạo ISO 15189 mời gọi 0919 099 777
Đọc thêm Bài giảng ISO 15189 và hướng dẫn áp dụng ISO 15189 tại đây
Xem các video Hướng dẫn áp dụng ISO 15189 tại đây
Đọc thêm kiểm tra xác nhận là gì (verification là gì) tại đây
#ISO15189 #baigiangiso15189 #huongdaniso15189 #tuvaniso15189 #daotaoiso15189 #iso15189:2022 #validate #xác nhận giá trị sử dụng




