NỘI DUNG
Bài giảng ISO 15189 và hướng dẫn áp dụng ISO 15189 yêu cầu 6.4 Thiết bị. Hướng dẫn và giải thích chi tiết cách áp dụng.
Yêu cầu 6.4.1 Tổng quát
Phòng xét nghiệm phải có quy trình lựa chọn, mua sắm, lắp đặt và nghiệm thu. Quy trình này bao gồm các tiêu chí về khả năng chấp nhận. Phòng xét nghiệm cũng cần có quy trình xử lý, vận chuyển, bảo quản, sử dụng, bảo trì và ngừng hoạt động của thiết bị. Quy trình này để đảm bảo thiết bị hoạt động bình thường. Nó cũng để ngăn ngừa nhiễm bẩn hoặc hư hỏng.
Giải thích
Yêu cầu này nhấn mạnh rằng phòng xét nghiệm cần có một hệ thống quản lý thiết bị toàn diện. Hệ thống này bao gồm tất cả các giai đoạn. Giai đoạn từ khi quyết định mua thiết bị cho đến khi thiết bị ngừng hoạt động. Điều này không chỉ giới hạn ở các máy móc xét nghiệm phức tạp. Nó còn bao gồm cả phần mềm, hệ thống đo lường, hệ thống thông tin và thậm chí cả thiết bị vận chuyển mẫu.
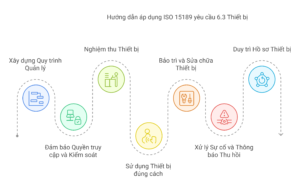
Hướng dẫn áp dụng
- Xây dựng một quy trình bằng văn bản. Quy trình này mô tả chi tiết từng bước quản lý thiết bị. Quy trình này từ lựa chọn, mua sắm, lắp đặt, nghiệm thu, sử dụng, bảo trì, đến khi loại bỏ thiết bị.
- Quy trình cần đảm bảo thiết bị luôn hoạt động tốt. Nó cũng cần đảm bảo sự ổn định trong suốt quá trình sử dụng.
- Quy trình cần có các biện pháp để bảo vệ thiết bị. Biện pháp này để bảo vệ thiết bị khỏi nhiễm bẩn, hư hỏng, sử dụng sai cách, hoặc bảo trì không đầy đủ.
- Xác định rõ phạm vi “thiết bị phòng xét nghiệm” trong quy trình của bạn. Nó không chỉ là máy xét nghiệm. Nó còn bao gồm tủ lạnh, máy ly tâm, pipet, phần mềm quản lý xét nghiệm (LIS), hệ thống đo lường, v.v.
Yêu cầu 6.4.2 Yêu cầu về thiết bị
a) Phòng xét nghiệm phải có quyền truy cập vào các thiết bị cần thiết. Thiết bị này để thực hiện chính xác các hoạt động của phòng xét nghiệm.
b) Trong trường hợp thiết bị được sử dụng nằm ngoài tầm kiểm soát thường xuyên của phòng xét nghiệm hoặc thông số chức năng kỹ thuật của nhà sản xuất, ban lãnh đạo phòng xét nghiệm phải đảm bảo rằng các yêu cầu của tài liệu này được đáp ứng.
c) Mỗi hạng mục của thiết bị có thể ảnh hưởng đến hoạt động của phòng xét nghiệm phải được dán nhãn riêng. Nó cũng cần được đánh dấu hoặc xác định duy nhất và duy trì sổ theo dõi.
d) Phòng xét nghiệm phải bảo dưỡng và thay thế thiết bị khi cần thiết. Việc này để đảm bảo chất lượng kết quả xét nghiệm.
Giải thích
Yêu cầu này nêu ra các điều kiện cần thiết về thiết bị. Điều kiện này để đảm bảo phòng xét nghiệm hoạt động hiệu quả. Nó cũng để cung cấp kết quả xét nghiệm đáng tin cậy.
Hướng dẫn áp dụng
a) Quyền truy cập thiết bị
- Xác định danh mục và số lượng thiết bị cần thiết. Việc xác định này dựa trên danh mục xét nghiệm, số lượng mẫu và công suất phòng xét nghiệm.
- Phải đảm bảo rằng phòng xét nghiệm luôn có đủ thiết bị hoạt động. Thiết bị này để thực hiện các xét nghiệm được cung cấp. Điều này có thể bao gồm việc mua sắm, thuê hoặc có thỏa thuận sử dụng chung thiết bị với đơn vị khác.
b) Thiết bị ngoài tầm kiểm soát
- Thiết bị sử dụng chung hoặc thuê: Nếu phòng xét nghiệm sử dụng thiết bị không thuộc quyền sở hữu hoặc quản lý trực tiếp (ví dụ sử dụng chung thiết bị với bệnh viện, thuê thiết bị), cần có biện pháp đảm bảo. Biện pháp này để thiết bị đó vẫn tuân thủ các yêu cầu của ISO 15189.
- Kiểm soát chất lượng: Thỏa thuận với đơn vị quản lý thiết bị về việc bảo trì, hiệu chuẩn, kiểm tra chất lượng thiết bị. Đảm bảo có hồ sơ chứng minh thiết bị được quản lý đúng cách.
c) Nhận diện và theo dõi thiết bị
- Gắn nhãn/đánh dấu: Mỗi thiết bị quan trọng (ví dụ máy xét nghiệm, tủ lạnh bảo quản mẫu, pipet định mức) cần được dán nhãn hoặc đánh dấu duy nhất. Việc này để dễ dàng nhận diện. Ví dụ “Máy Sinh hóa – Số 01”.
- Sổ theo dõi thiết bị: Lập sổ theo dõi. Sổ này có thể là sổ giấy hoặc hệ thống điện tử. Sổ này để ghi lại thông tin chi tiết về từng thiết bị (như mô tả ở mục 6.4.7).
d) Bảo dưỡng và thay thế
- Lập kế hoạch bảo dưỡng: Dựa trên hướng dẫn của nhà sản xuất và kinh nghiệm sử dụng, xây dựng kế hoạch bảo dưỡng định kỳ cho từng loại thiết bị. Kế hoạch cần nêu rõ các công việc bảo trì cần thực hiện, tần suất và người thực hiện.
- Theo dõi tình trạng thiết bị: Thường xuyên kiểm tra tình trạng hoạt động của thiết bị.
- Thay thế khi cần thiết: Khi thiết bị xuống cấp, hỏng hóc thường xuyên, hoặc không còn đáp ứng yêu cầu xét nghiệm, cần có kế hoạch thay thế kịp thời. Việc thay thế này để đảm bảo chất lượng xét nghiệm không bị ảnh hưởng.
Yêu cầu 6.4.3 Thủ tục nghiệm thu thiết bị
Phòng xét nghiệm phải xác minh rằng thiết bị phù hợp với các tiêu chí chấp nhận được xác định trước. Việc xác minh này cần thực hiện trước khi đưa thiết bị vào sử dụng hoặc khi đưa trở lại sử dụng.
Thiết bị được sử dụng để đo phải có khả năng đạt được độ chính xác của phép đo hoặc độ không đảm bảo đo, hoặc cả hai. Độ chính xác hoặc độ không đảm bảo đo này được yêu cầu để cung cấp kết quả hợp lệ (xem 7.3.3 và 7.3.4 để biết chi tiết).
Giải thích
Yêu cầu này nhấn mạnh tầm quan trọng của việc nghiệm thu thiết bị trước khi sử dụng. Việc nghiệm thu này để đảm bảo thiết bị hoạt động đúng như mong đợi và phù hợp với mục đích sử dụng.
Hướng dẫn áp dụng
- Xác định tiêu chí chấp nhận: Trước khi nghiệm thu, phòng xét nghiệm cần xác định rõ các tiêu chí chấp nhận cho từng loại thiết bị. Tiêu chí này có thể dựa trên thông số kỹ thuật của nhà sản xuất, yêu cầu về độ chính xác của xét nghiệm, hoặc các quy định của pháp luật. Ví dụ, tiêu chí chấp nhận cho máy phân tích huyết học có thể bao gồm độ chính xác và độ lặp lại của các thông số huyết học, chức năng hoạt động của hệ thống, v.v.
- Thủ tục nghiệm thu: Xây dựng quy trình nghiệm thu chi tiết. Quy trình này bao gồm các bước kiểm tra, thử nghiệm và các tiêu chí đánh giá.
- Thực hiện nghiệm thu: Tiến hành nghiệm thu theo quy trình đã xây dựng. Việc nghiệm thu này khi thiết bị mới được mua, sau khi sửa chữa lớn, hoặc sau khi di chuyển thiết bị đến vị trí mới.
- Ghi lại kết quả nghiệm thu: Lập hồ sơ nghiệm thu. Hồ sơ này ghi lại kết quả kiểm tra, thử nghiệm và so sánh với tiêu chí chấp nhận. Hồ sơ nghiệm thu phải được lưu giữ.
- Thiết bị đo lường: Đối với các thiết bị đo lường (ví dụ pipet, cân phân tích), cần đảm bảo chúng có khả năng đạt được độ chính xác hoặc độ không đảm bảo đo cần thiết cho xét nghiệm. Có thể dựa vào chứng nhận hiệu chuẩn để xác minh điều này.
- Thiết bị bên ngoài phòng xét nghiệm: Yêu cầu này cũng áp dụng cho thiết bị sử dụng bên ngoài phòng xét nghiệm. Thiết bị này nhưng thuộc phạm vi quản lý của phòng xét nghiệm (ví dụ thiết bị xét nghiệm tại giường bệnh, thiết bị xét nghiệm lưu động).
Ví dụ
- Máy phân tích sinh hóa mới: Khi mua máy phân tích sinh hóa mới, phòng xét nghiệm xây dựng quy trình nghiệm thu. Quy trình này bao gồm:
- Kiểm tra ngoại quan và các phụ kiện đi kèm.
- Chạy kiểm tra các chức năng cơ bản của máy. Ví dụ hệ thống hút mẫu, hệ thống rửa, hệ thống quang học.
- Chạy mẫu kiểm tra chất lượng (QC) và mẫu chuẩn. Việc này để đánh giá độ chính xác và độ lặp lại của các xét nghiệm.
- So sánh kết quả với tiêu chí chấp nhận đã xác định. Ví dụ CV% của QC phải < 5%, độ lệch so với giá trị chuẩn < 10%.
- Lập biên bản nghiệm thu nếu tất cả các tiêu chí đều đạt.
Cần tư vấn đào tạo ISO 15189 mời gọi 0919 099 777
Yêu cầu 6.4.4 Hướng dẫn sử dụng thiết bị
a) Phòng xét nghiệm phải có các biện pháp bảo vệ thích hợp. Biện pháp này để ngăn chặn các điều chỉnh ngoài ý muốn của thiết bị. Điều chỉnh này có thể làm mất hiệu lực của kết quả xét nghiệm.
b) Thiết bị phải được vận hành bởi nhân viên được đào tạo, được ủy quyền và có năng lực.
c) Hướng dẫn sử dụng thiết bị, bao gồm cả hướng dẫn thiết bị do nhà sản xuất cung cấp, phải có sẵn.
d) Thiết bị phải được sử dụng theo quy định của nhà sản xuất, trừ khi được xác nhận bởi phòng xét nghiệm (xem 7.3.3).
Giải thích
Yêu cầu này đảm bảo rằng thiết bị được sử dụng đúng cách, bởi người có năng lực và theo hướng dẫn. Việc này để đảm bảo kết quả xét nghiệm tin cậy.
Hướng dẫn áp dụng
a) Ngăn chặn điều chỉnh ngoài ý muốn
- Cài đặt bảo mật: Đối với các thiết bị có phần mềm điều khiển, thiết lập mật khẩu hoặc phân quyền người dùng. Việc này để hạn chế quyền truy cập và thay đổi cài đặt quan trọng.
- Khóa các nút điều chỉnh: Đối với các thiết bị có các nút điều chỉnh vật lý, có thể sử dụng các biện pháp khóa hoặc niêm phong. Biện pháp này để ngăn chặn việc vô tình thay đổi cài đặt.
- Quy trình thao tác chuẩn (SOP): Xây dựng SOP chi tiết. SOP này hướng dẫn cách sử dụng thiết bị. Trong SOP cần quy định rõ các thông số cài đặt chuẩn và các bước thao tác để tránh việc điều chỉnh sai lệch.
b) Nhân viên được đào tạo và có năng lực
- Đào tạo: Tổ chức đào tạo cho nhân viên về cách sử dụng, bảo trì và xử lý sự cố cơ bản của thiết bị. Đào tạo có thể do nhà sản xuất, người có kinh nghiệm trong phòng xét nghiệm hoặc các đơn vị đào tạo chuyên nghiệp thực hiện.
- Đánh giá năng lực: Sau đào tạo, đánh giá năng lực của nhân viên. Việc đánh giá này để đảm bảo họ có đủ kiến thức và kỹ năng. Kỹ năng để vận hành thiết bị an toàn và hiệu quả.
- Ủy quyền: Chỉ những nhân viên đã được đào tạo và đánh giá năng lực đạt yêu cầu mới được ủy quyền sử dụng thiết bị.
c) Hướng dẫn sử dụng có sẵn
- Hướng dẫn của nhà sản xuất: Luôn giữ sẵn hướng dẫn sử dụng gốc của nhà sản xuất. Hướng dẫn này có thể là bản in hoặc bản điện tử. Hãy giữ tại nơi làm việc.
- Hướng dẫn sử dụng của phòng xét nghiệm: Xây dựng hướng dẫn sử dụng riêng của phòng xét nghiệm. Hướng dẫn này có thể đơn giản hóa hoặc cụ thể hóa hơn hướng dẫn của nhà sản xuất. Nó cần phù hợp với quy trình và điều kiện thực tế của phòng xét nghiệm.
- Dễ dàng tiếp cận: Đảm bảo nhân viên dễ dàng tiếp cận các hướng dẫn sử dụng khi cần thiết.
d) Sử dụng theo hướng dẫn của nhà sản xuất
- Tuân thủ hướng dẫn: Ưu tiên sử dụng thiết bị theo đúng hướng dẫn của nhà sản xuất.
- Xác nhận khi có thay đổi: Nếu phòng xét nghiệm muốn thay đổi quy trình sử dụng so với hướng dẫn của nhà sản xuất (ví dụ thay đổi thông số xét nghiệm, quy trình bảo trì), cần phải thực hiện xác nhận (validation). Việc xác nhận này để chứng minh rằng sự thay đổi này không ảnh hưởng tiêu cực đến kết quả xét nghiệm. (Xem thêm yêu cầu 7.3.3 về xác nhận quy trình xét nghiệm).
6.4.5 Bảo dưỡng và sửa chữa thiết bị
Yêu cầu
a) Phòng xét nghiệm phải có các chương trình bảo trì phòng ngừa. Chương trình này dựa trên hướng dẫn của nhà sản xuất. Những sai lệch so với lịch trình hoặc hướng dẫn của nhà sản xuất phải được ghi lại.
b) Thiết bị phải được duy trì trong điều kiện làm việc an toàn và hoạt động bình thường. Điều này phải bao gồm an toàn điện, bất kỳ thiết bị dừng khẩn cấp nào và việc xử lý và tiêu hủy an toàn các vật liệu nguy hiểm bởi nhân viên được uỷ quyền.
c) Thiết bị bị lỗi hoặc không đạt yêu cầu quy định sẽ bị ngừng sử dụng. Nó phải được dán nhãn rõ ràng hoặc đánh dấu là không hoạt động. Việc này cho đến khi nó được xác minh là hoạt động chính xác. Phòng xét nghiệm phải xem xét ảnh hưởng của lỗi hoặc sai lệch so với các yêu cầu quy định. Phòng xét nghiệm cũng phải bắt đầu các hành động khi xảy ra sự không phù hợp (xem 7.5).
d) Khi có thể, phòng xét nghiệm phải khử nhiễm thiết bị trước khi bảo dưỡng, sửa chữa hoặc ngừng hoạt động. Phòng xét nghiệm cũng cần cung cấp không gian thích hợp để sửa chữa và cung cấp thiết bị bảo hộ cá nhân thích hợp.
Giải thích
Yêu cầu này tập trung vào việc duy trì thiết bị ở trạng thái hoạt động tốt, an toàn và xử lý các sự cố một cách hiệu quả.
Hướng dẫn áp dụng
a) Chương trình bảo trì phòng ngừa
- Lập kế hoạch bảo trì: Dựa trên hướng dẫn của nhà sản xuất, xây dựng kế hoạch bảo trì phòng ngừa định kỳ cho từng loại thiết bị. Ví dụ hàng ngày, hàng tuần, hàng tháng, hàng năm. Kế hoạch cần nêu rõ các công việc bảo trì cần thực hiện, tần suất và người thực hiện.
- Thực hiện bảo trì: Thực hiện bảo trì theo kế hoạch đã lập.
- Ghi lại hoạt động bảo trì: Ghi lại chi tiết các hoạt động bảo trì đã thực hiện. Ví dụ ngày thực hiện, công việc, người thực hiện, kết quả kiểm tra sau bảo trì, v.v. Ghi vào hồ sơ thiết bị.
- Xử lý sai lệch: Nếu có bất kỳ sai lệch nào so với lịch trình hoặc hướng dẫn của nhà sản xuất (ví dụ không thực hiện bảo trì đúng hạn, thay đổi quy trình bảo trì), cần ghi lại lý do và đánh giá ảnh hưởng của sai lệch.
b) Điều kiện làm việc an toàn và bình thường
- An toàn điện: Kiểm tra định kỳ hệ thống điện của thiết bị để đảm bảo an toàn. Ví dụ dây điện không bị hở, tiếp đất tốt.
- Thiết bị dừng khẩn cấp: Đảm bảo các thiết bị có nút dừng khẩn cấp (nếu có) hoạt động tốt và dễ dàng tiếp cận.
- Xử lý vật liệu nguy hiểm: Xây dựng quy trình an toàn cho việc xử lý và tiêu hủy các vật liệu nguy hiểm. Vật liệu này phát sinh từ quá trình sử dụng thiết bị. Ví dụ hóa chất thải, vật tư tiêu hao nhiễm khuẩn. Đảm bảo nhân viên được đào tạo và trang bị đầy đủ phương tiện bảo hộ cá nhân (PPE).
c) Thiết bị lỗi hoặc không đạt yêu cầu
- Ngừng sử dụng: Khi phát hiện thiết bị bị lỗi hoặc không đạt yêu cầu (ví dụ kết quả QC không đạt, máy báo lỗi), phải ngừng sử dụng thiết bị ngay lập tức.
- Dán nhãn/đánh dấu: Dán nhãn hoặc đánh dấu rõ ràng thiết bị là “KHÔNG HOẠT ĐỘNG” hoặc “ĐANG HƯ HỎNG”. Việc này để tránh sử dụng nhầm.
- Sửa chữa và xác minh: Chỉ đưa thiết bị trở lại sử dụng sau khi đã được sửa chữa và xác minh là hoạt động chính xác. Ví dụ kiểm tra lại chức năng, chạy QC.
- Xem xét ảnh hưởng và hành động khắc phục: Đánh giá xem lỗi thiết bị có thể ảnh hưởng đến các kết quả xét nghiệm đã thực hiện hay không. Nếu có, cần thực hiện các hành động khắc phục phù hợp. Ví dụ xem xét lại kết quả, thông báo cho bác sĩ lâm sàng, xét nghiệm lại mẫu nếu cần. (Xem thêm yêu cầu 7.5 về hành động khắc phục).
d) Khử nhiễm, không gian và PPE
- Khử nhiễm: Trước khi bảo dưỡng, sửa chữa hoặc ngừng hoạt động thiết bị, nếu có thể, hãy khử nhiễm thiết bị. Việc khử nhiễm này để đảm bảo an toàn cho nhân viên bảo trì, sửa chữa.
- Không gian sửa chữa: Cung cấp không gian làm việc phù hợp, đủ ánh sáng, thông thoáng và an toàn cho việc sửa chữa thiết bị.
- PPE: Cung cấp đầy đủ PPE phù hợp cho nhân viên thực hiện bảo dưỡng, sửa chữa. Ví dụ găng tay, kính bảo hộ, khẩu trang, áo choàng.
Cần tư vấn đào tạo ISO 15189 mời gọi 0919 099 777
Yêu cầu 6.4.6 Báo cáo sự cố bất lợi của thiết bị
Các sự cố và tai nạn bất lợi có thể được quy trực tiếp cho thiết bị cụ thể sẽ được điều tra. Sự cố và tai nạn này cũng sẽ được báo cáo cho nhà sản xuất hoặc nhà cung cấp, hoặc cả hai, và các cơ quan có thẩm quyền thích hợp, theo yêu cầu.
Phòng xét nghiệm phải có các thủ tục để ứng phó với bất kỳ thông báo thu hồi hoặc thông báo nào khác của nhà sản xuất. Phòng xét nghiệm cũng cần thực hiện các hành động do nhà sản xuất khuyến nghị.
Giải thích
Yêu cầu này đảm bảo rằng các sự cố nghiêm trọng liên quan đến thiết bị được xử lý một cách có hệ thống. Việc xử lý này bao gồm việc báo cáo cho các bên liên quan và thực hiện các hành động cần thiết.
Hướng dẫn áp dụng
- Điều tra sự cố: Khi có sự cố bất lợi liên quan đến thiết bị (ví dụ máy hoạt động sai, gây ra kết quả sai, gây tai nạn cho nhân viên), cần tiến hành điều tra. Việc điều tra này để xác định nguyên nhân gốc rễ.
- Báo cáo sự cố
- Nhà sản xuất/nhà cung cấp: Báo cáo sự cố cho nhà sản xuất hoặc nhà cung cấp thiết bị. Việc báo cáo này đặc biệt là khi sự cố có thể liên quan đến lỗi thiết kế, lỗi sản xuất, hoặc cần hỗ trợ kỹ thuật từ nhà sản xuất.
- Cơ quan có thẩm quyền: Nếu có yêu cầu của pháp luật hoặc quy định, báo cáo sự cố cho các cơ quan quản lý nhà nước có liên quan. Ví dụ Sở Y tế, Bộ Y tế.
- Thủ tục ứng phó với thông báo thu hồi
- Theo dõi thông tin thu hồi: Thiết lập cơ chế theo dõi thông tin thu hồi sản phẩm, cảnh báo an toàn từ nhà sản xuất và các cơ quan quản lý. Có thể đăng ký nhận thông tin từ website của nhà sản xuất hoặc các tổ chức y tế.
- Thực hiện hành động thu hồi: Khi nhận được thông báo thu hồi thiết bị, cần thực hiện ngay các hành động theo khuyến cáo của nhà sản xuất. Ví dụ ngừng sử dụng thiết bị, kiểm tra lô sản phẩm bị ảnh hưởng, thay thế linh kiện, trả lại thiết bị cho nhà sản xuất.
- Lưu hồ sơ: Lưu giữ hồ sơ về các sự cố đã báo cáo, các thông báo thu hồi đã nhận được và các hành động đã thực hiện để ứng phó.
Ví dụ
- Thông báo thu hồi: Nhà sản xuất máy xét nghiệm đông máu gửi thông báo thu hồi một lô hóa chất đông máu do phát hiện lỗi sản xuất. Lỗi sản xuất này có thể ảnh hưởng đến kết quả xét nghiệm PT và APTT. Phòng xét nghiệm kiểm tra lô hóa chất đang sử dụng, xác định có lô bị thu hồi, lập tức ngừng sử dụng lô hóa chất này, liên hệ nhà cung cấp để đổi lô mới và xem xét lại các kết quả xét nghiệm đông máu đã thực hiện bằng lô hóa chất bị lỗi. Việc xem xét này để đánh giá ảnh hưởng và có hành động phù hợp.
Yêu cầu 6.4.7 Hồ sơ thiết bị
Hồ sơ phải được duy trì cho từng hạng mục thiết bị. Thiết bị này ảnh hưởng đến kết quả hoạt động của phòng xét nghiệm.
Các hồ sơ này phải được lưu giữ. Chúng cũng phải có sẵn trong suốt vòng đời của thiết bị hoặc lâu hơn, như được quy định trong 8.4.3.
Giải thích
Yêu cầu này quy định về việc lưu giữ hồ sơ chi tiết cho từng thiết bị. Việc lưu giữ này để đảm bảo khả năng truy xuất nguồn gốc, theo dõi lịch sử hoạt động, bảo trì và hiệu suất của thiết bị. Hồ sơ thiết bị là một phần quan trọng của hệ thống quản lý chất lượng phòng xét nghiệm.
Hướng dẫn áp dụng
- Lập hồ sơ cho từng thiết bị
- Tên thiết bị, model, số serial, nhà sản xuất, nhà cung cấp, ngày mua, ngày đưa vào sử dụng, vị trí đặt, tình trạng thiết bị khi mua (mới, cũ, tân trang).
- Biên bản nghiệm thu thiết bị, hồ sơ nghiệm thu, chứng nhận thiết bị đạt tiêu chí chấp nhận.
- Hướng dẫn sử dụng của nhà sản xuất, chương trình bảo dưỡng phòng ngừa.
- Lịch sử bảo trì (ngày thực hiện, công việc, người thực hiện), hồ sơ sửa chữa (mô tả sự cố, biện pháp sửa chữa, ngày sửa chữa, người sửa chữa).
- Hồ sơ hiệu chuẩn (giấy chứng nhận hiệu chuẩn, báo cáo hiệu chuẩn), hồ sơ kiểm tra xác nhận (ví dụ kết quả kiểm tra chất lượng nội kiểm, ngoại kiểm).
- Ghi lại tình trạng hiện tại của thiết bị. Ví dụ đang hoạt động, ngừng hoạt động, chờ sửa chữa, đã loại bỏ.
Tóm tắt Yêu cầu 6.4 Thiết bị
Yêu cầu 6.4 trong ISO 15189:2022 về Thiết bị tập trung vào việc đảm bảo phòng xét nghiệm quản lý thiết bị một cách toàn diện và hiệu quả. Việc quản lý này từ khâu lựa chọn, mua sắm, sử dụng, bảo trì đến khi loại bỏ. Mục tiêu chính là đảm bảo thiết bị luôn hoạt động tốt, an toàn và cung cấp kết quả xét nghiệm chính xác và tin cậy.
Các điểm chính cần lưu ý
- Quy trình quản lý thiết bị toàn diện: Xây dựng và tuân thủ quy trình quản lý thiết bị cho tất cả các giai đoạn.
- Đảm bảo quyền truy cập và kiểm soát thiết bị: Phải có đủ thiết bị cần thiết và kiểm soát được chất lượng thiết bị. Việc này kể cả khi sử dụng thiết bị bên ngoài phòng xét nghiệm.
- Nghiệm thu thiết bị trước khi sử dụng: Xác minh thiết bị đáp ứng các tiêu chí chấp nhận trước khi đưa vào sử dụng.
- Sử dụng thiết bị đúng cách: Đảm bảo nhân viên được đào tạo, có hướng dẫn sử dụng và tuân thủ hướng dẫn của nhà sản xuất.
- Bảo trì và sửa chữa thiết bị định kỳ: Thực hiện bảo trì phòng ngừa và sửa chữa kịp thời. Việc này để duy trì thiết bị ở trạng thái tốt.
- Xử lý sự cố và thông báo thu hồi: Có quy trình báo cáo và ứng phó với các sự cố thiết bị và thông báo thu hồi từ nhà sản xuất.
- Lưu giữ hồ sơ thiết bị đầy đủ: Duy trì hồ sơ chi tiết cho từng thiết bị. Việc này để theo dõi lịch sử và hiệu suất của thiết bị.
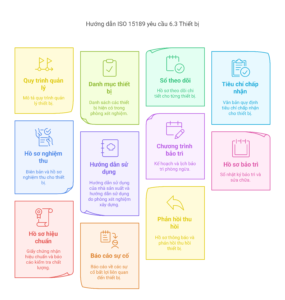
Hồ sơ cần chứng minh tuân thủ Yêu cầu 6.4
Để chứng minh phòng xét nghiệm của bạn tuân thủ Yêu cầu 6.4 về Thiết bị, bạn cần chuẩn bị và duy trì các hồ sơ sau:
- Quy trình quản lý thiết bị
- Danh mục thiết bị
- Sổ theo dõi thiết bị
- Tiêu chí chấp nhận thiết bị
- Hồ sơ nghiệm thu thiết bị
- Hướng dẫn sử dụng thiết bị
- Chương trình bảo trì phòng ngừa
- Hồ sơ bảo trì và sửa chữa thiết bị
- Hồ sơ hiệu chuẩn/kiểm tra xác nhận .
- Hồ sơ báo cáo sự cố thiết bị
- Hồ sơ ứng phó với thông báo thu hồi
Trí Phúc
Cần tư vấn đào tạo ISO 15189 mời gọi 0919 099 777
Đọc thêm Bài giảng ISO 15189 và hướng dẫn áp dụng ISO 15189 tại đây
Xem các video Hướng dẫn áp dụng ISO 15189 tại đây
#ISO15189 #baigiangiso15189 #huongdaniso15189 #tuvaniso15189 #daotaoiso15189 #iso15189:2022
.